国内首个原研“减肥针”获准,每天都要打3针
7月27根据国家医药产品管理局的规定,(NMPA)医疗器械许可证材料发送信息显示,仁会生物贝那鲁肽注射剂获准新适应症。
据仁会生物官网消息,此次获准适应症为超重/肥胖,适用于BMI。 ≥ 28kg/m² 者,或 BMI ≥ 24kg/m²与体重相关的并发症至少有一种(如高血糖、高血压、高脂血症、脂肪肝、阻塞性睡眠呼吸暂停综合征等),规格为 4.2mg(42000U)(2.1ml)/支。

到目前为止,国内首次获准原研究。「减肥针」正式诞生。
01 第一种原研药物,利拉鲁肽之前被批准为生物类似药物
7 月初,同为持续火爆的月初。 GLP-1 中美华东的利拉鲁肽注射剂类药物刚刚被斩获「减肥针」国内首个上市许可证。2020年,利拉鲁肽原研方为丹麦药企诺和诺德。 2008年以后,各类专利陆续到期,首次获准。「减肥针」就是它的生物相似药物。
而且后来刚刚获准的贝那鲁肽是 1 类药,是仁会生物的原研产品。
GLP-1 它是一种促进胰岛素分泌、抑制胰高糖素分泌、降低血糖、减缓胃排空、抑制食欲的肠促胰素。它是一种肠促胰素。
利拉鲁肽最早是由诺和诺德开发的。 2009 年于欧盟 2 糖尿病药物上市。2014 年 12 月,美国 FDA 准许其「超重或肥胖」新的适应症,开创了 GLP-1 用于超重、肥胖治疗的先河药物。
主流如利拉鲁肽、司美格鲁肽等 GLP-1 不同的受体激动剂类药物,贝那鲁肽和人类 GLP-1 同样的氨基酸序列,通过基因工程串联表达技术制备[1]。
贝那鲁肽Ⅲ 期临床试验于 2019 年度申请获准,是国家重大科技专项 09 重点(重大新药创作技术重大专项)是中国第一个减肥领域的注册临床试验,也是世界上第一个全人源 GLP-1 类药减重临床试验[2]。
入组的 434 名受试者,BMI ≥ 28kg/m²,或BMI ≥ 24kg/m² 还有以下至少一种表现:食欲旺盛, 饭前饥饿难忍,每顿饭吃得更多;合并一种或多种高血糖、高血压、高脂血症和脂肪肝;合并重量关节痛;肥胖导致呼吸不畅或阻塞性睡眠呼吸暂停综合征。
选用规格 2.1ml:4.2mg贝那鲁肽皮内注射(42000U);一天三次(TID),起始剂量为 0.06mg TID,逐步调整达到目标剂量 0.2mg TID。
试验的主要终点设置是 16 与基线平均值相比,周时治疗组和安慰剂组的体重降低了百分比差,至少减轻了体重。 比较5%。[3]
2021 年 10 月 26 日,该 Ⅲ 期临床试验通过国家卫生健康委医疗卫生科技发展研究中心综合绩效评估,未公布结果的实际数据[2]。
02 现实世界研究:3 个月减重 12.9%
贝那鲁肽 2017 年作为 2 糖尿病治疗药物上市后,Obesityy发表了一项关于减肥的真实世界研究。 Science &Practice。虽然回顾性和观察性的研究在循证医学体系中证据水平较低,但在真实的诊断和治疗环境中可以看到减肥的具体疗效。[4,5]。
这项研究被列入中国两个中心 314 例 2 糖尿病患者,平均体重 77.94kg,BMI 均值为 27.95kg/m²。
病人在常规诊疗环境中接受治疗,215 给贝那鲁肽单药,96 贝那鲁肽与甘精胰岛素结合,例如3 二甲双胍在上述两种方案的基础上联合使用。1~经过两周的定期剂量滴滴,超过三分之二的病人贝那鲁肽日剂量 ≥ 0.3mg,大约二分之一的病人贝那鲁肽日剂量 ≥ 0.48mg。
减肥方面的数据显示,治疗前后贝那鲁肽平均体重下降。 10.05kg,平均体重下降百分比 比基线体重减轻12.90%以上 5% 和 10% 患者各自达到 84.96%、72.18%。
现在我们国家已经批准减肥 GLP-1 利拉鲁肽和贝那鲁肽是唯一的药物。
利拉鲁肽3 项 Ⅲ 临床试验表明,比基线体重减轻 5% 和 10% 患者比例分别为 60% 和三分之一[6]。
其中,最大样本(包括 3731 一个例子病人)的历时 56 星期,对象是年龄 ≥ 18 年龄,无糖尿病,BMI ≥ 30kg/m²(或 BMI ≥ 27kg/m² 患有高脂血症或高血压等肥胖症的患者,剂量为3mg/天,同时接受生活方式干预[7]。
03 每天都需要半衰期短 3 针,或新增「皮下泵」给药方式
利拉鲁肽和贝那鲁肽都是短效制剂,利拉鲁肽半衰期 12~14 小时,1 天 1 针; 半衰期只有贝那鲁肽 15 分钟,1 天需打 3 针,也就是类似胰岛素的「随餐给药」。
据仁会生物官网介绍,贝那鲁肽 「 随餐给药,模拟自然 GLP-1 分泌更符合正常人的生理节律。」;「 见效快,半衰期短,用药后代谢快,不在体内累积或长时间滞留, 常见的不良反应,如腹胀、恶心等,持续时间较短,水平较轻 」。[8]
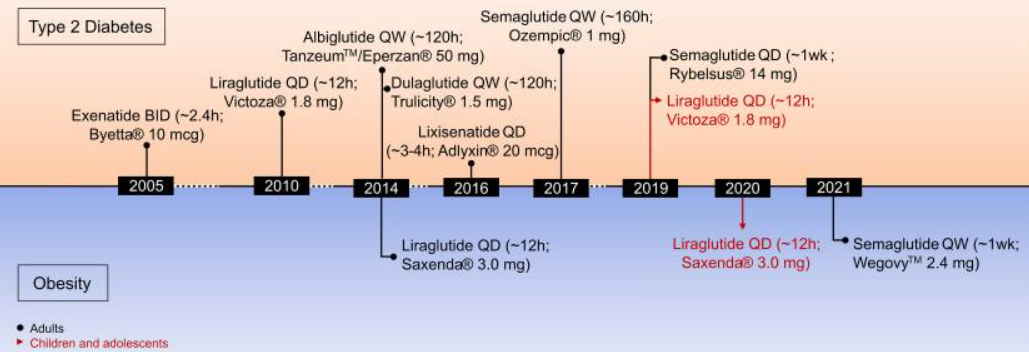
但是另一方面,肥胖症需要长期的管理,停药后容易反弹,频繁使用药物的依从性问题也会影响药物的选择和实际效果。从原形 GLP-1 到 GLP-1 受体激动剂药代动力学的特点不断完善,半衰期从天然激素中约2~3 一天发展两次(艾塞那肽 BID)、一天一次(利拉鲁肽、利西那肽),甚至一周一次(艾赛那肽 ER、阿必鲁肽,度拉糖肽,司美格鲁肽)[9]。
目前,一片红海,风靡全球。 GLP-1 从R&D风向来看,半衰期较长、微创(口服)的给药方式,似乎是更主流的发展趋势。
最火「减肥针」司美格鲁肽注射剂,保持剂量为 2.4mg,每周 1 次,根据 Ⅲb 临床试验结果 68 周减重率为 15.8% [10]。司美格鲁肽开发的口服制剂也发布了用于减肥的口服制剂 Ⅲ临床试验结果,常规剂量为 14mg,每天 1 次[11]。
今年 6 月亮,礼来的retatrutide创造了一个快速减肥记录(48 每周最高24.2%[12]。而且很短 1 月亮过后,礼物来了 7 月 27 每天再次披露,另一种药物替尔泊肽研究,84 周减重率达 26.6%[13]。
礼来的两种新药堪比减肥手术,与司美格鲁肽同为周制剂。安进正在研究的双特异性抗体多肽偶联物 AMG133 那么效果更长,每个月只需要给药 1 次[14]。
贝那鲁肽作为糖尿病治疗药物上市后,一直是仁会生物的核心产品,已经纳入国家医疗保险,但销售情况似乎不如预期。根据仁会生物官网公布的年报,2017年 年至 2019 年度销售额分别为 1360.71 万元、2681.69 万元和 5588.08 万元[15]。
另一方面,当时已经有现象级产品司美格鲁肽的诺和诺德,2019 年度中国区收入 125.10 亿丹麦克朗(约 128.97 亿元),占糖尿病市场的一亿元 27.4%;GLP-1 业务收入为8.98 亿丹麦克朗(约 9.26 亿元),占 GLP-1 市场的 92.8%[16]。
针对人内源 GLP-1 仁会生物曾经借鉴胰岛素泵对半衰期短的问题进行了尝试[17]。
「选择人工智能控制的药物输入泵设备,借鉴速效胰岛素皮下泵给药方法,可方便持续给药,充分发挥贝那鲁肽的临床价值。」在 Ⅲ 在临床试验后期,仁会生物补充申请泵给药方式, 2021 年 6 月 3 日获准许。[17]
国内减肥市场规模正在快速增长,从 2016 年不到 3 亿元,增至 2020 年 19 复合年增长率为亿元 预计64.6% 2025 这个数字将在2008年实现 87 并将保持高速增长至亿元, 2030 年达149 亿元。[18]
减重率高,安全,长效,微创,「减肥药」发展趋势将更加明朗,百亿国内市场竞争方兴,谁将真正满足市场需求,成为下一个赢家?
本文来自微信微信官方账号“丁香园”(ID:dingxiangwang),作家:丁香园 DXY,36氪经授权发布。
本文仅代表作者观点,版权归原创者所有,如需转载请在文中注明来源及作者名字。
免责声明:本文系转载编辑文章,仅作分享之用。如分享内容、图片侵犯到您的版权或非授权发布,请及时与我们联系进行审核处理或删除,您可以发送材料至邮箱:service@tojoy.com




