探序秩元自研生物结构预测基础模型,欲打破新药研发双十定律
一直以来,科学研究都以数学原理和实验观测为基础。从牛顿的《自然哲学的数学原理》到爱因斯坦的质能方程,科学家们依靠公式、定律、实验和精确计算来理解和预测自然。
如今,随着生成式人工智能的发展,特别是Transformer和Diffusion模型在文本、多模态等领域取得显著成果,“生成式科学”有望改变传统的科学研究范式。它不再局限于对每个中间步骤进行精确的数学描述和实验验证,而是借助海量科学数据(如基因序列、结构等)进行基石模型训练,直接生成结果,以实现“相对准、绝对快、绝对广”的更好效果。
“生成式科学”真正的开端是AlphaFold 2的诞生,它革命性地解决了蛋白质“从序列到结构”的预测问题。2023年,AlphaFold 3发布,其能力扩展到蛋白质与核酸、小分子、抗体等复杂生物分子的相互作用,使AF3具备了指导药物研发的潜力。
2024年初,Deepmind旗下负责AF3产业化的子公司Isomorphic Labs,从礼来、诺华两家跨国制药公司获得巨额订单,合作开发多靶点的小分子疗法,预付款分别高达4500万美元、3750万美元。2025年初,诺华宣布拓展与Isomorphic Labs的合作,增加合作研究数量,这表明诺华认可其探索“未公开靶点”药物的能力。
36氪了解到,2024年下半年成立的新创公司探序秩元(以下简称探序),在生成式科学的浪潮中,发布了自研基础模型IntelliFold,目前已开放公开server。
创始人孙鹏曾是tech venture投资人,职业生涯始于Accenture管理咨询,后在明势资本等VC机构任职,有丰富的AI投资与产业经营经验;首席科学家孙思琦是复旦大学研究员、博士生导师,在芝加哥大学TTI - Chicago读博时师从许锦波教授。2018 - 2022年,孙思琦在微软西雅图总部从事前沿大语言模型技术研究,回国后致力于AI在交叉学科的创新应用,在结构生物学智能计算领域取得系统性前沿突破,成果发表于Science、Nature子刊等顶级期刊,总引用超过7000次。
孙鹏向36氪介绍,探序秩元的科研团队成员大多具备“结构生物学 + 大语言模型”双重研发背景,因此有能力自主开发结构预测基础模型。
孙鹏表示:“几年前,AI对结构生物学的结合预测和设计任务主要是提升效率;现在要用新的AI解决传统技术难以解决的问题,如高效探索未公开靶点,设计全新产物等,AI大模型不可或缺。我们所做的事,不像训练通用大语言模型那样消耗大量算力,且产业价值转化路径更短、更明确。用生成式科学模型直接参与科学研究探索,是AGI展开为智能生产力的三个一级切入点之一。”
据悉,IntelliFold定位为“可控的基础模型”。一方面,它能对多种生物分子(蛋白质、核酸、小分子、离子、修饰残基等)之间的相互作用进行高精度三维结构预测;另一方面,通过应用轻量级的可训练适配器,它能被引导和控制,实现别构预测、给定口袋结合预测等特定能力,帮助完成药物发现等下游应用的复杂任务。
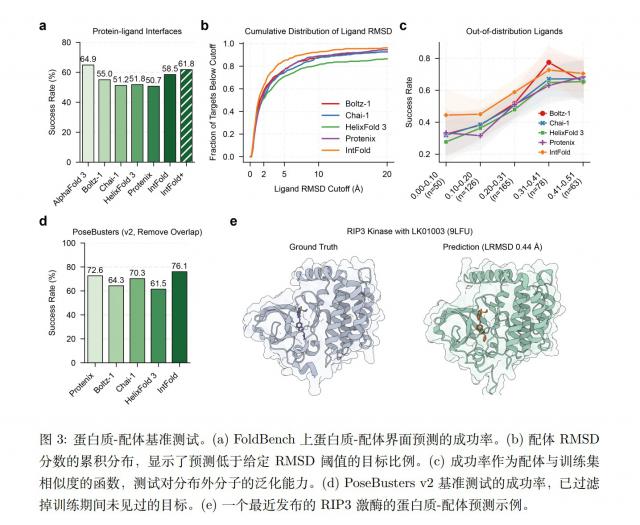
图源报告:《IntelliFold:一个用于通用和特化生物分子结构预测的可控基础模型》
公司提供的技术测试报告显示,IntelliFold在蛋白质结构预测测试的多个关键指标上与AF3表现相当,如蛋白质单体结构预测、蛋白质 - 蛋白质界面预测、蛋白质 - DNA/RNA界面等。在抗体 - 抗原界面、蛋白质 - 配体相互作用预测方面,成功率略低于AF3。值得注意的是,在RNA单体预测上,它超越了AF3,展现了在核酸结构预测上的优势。
孙鹏称:“给定具体蛋白质序列,IntelliFold模型可以预测它与小分子的结合构象及模式,这是我们当前技术的特点,也是市场有明确需求的方向之一。除预测别构等特异性结合模式外,IntelliFold模型还能预测Affinity(结合亲和力,衡量药物效力的核心指标之一)数值,可增强药物虚拟筛选的效率和准确性。”
在药物设计中,蛋白质会因结合分子产生构象变化,形成不同功能状态,如激酶家族中的CDK2,其活性可能受抑制剂诱导的别构变化影响。这对药物设计很重要,但在大模型中难以有效训练。通过目标特异性适配器,IntelliFold能正确预测别构构象,“识别罕见构象状态,同时不影响模型在正构状态上的准确性”,这对药物精准设计的灵活性很关键。
孙鹏还提到,生成式科学模型正在快速改变蛋白质设计。与经典的专家主导药物设计范式不同,生成式模型可以完全从头设计每一个氨基酸的位置及可能性,甚至探索自然界不存在但可能更优的结果。“虽然蛋白质从头设计和结合预测的难点不同,但二者使用的基石模型相近,具备横向拓展能力。基石模型能力是未来在具体场景取得领先性和产业可用性的关键前提。”
探序秩元未来希望将IntelliFold打造成通用的智能科学基石模型,在不同任务中发挥引擎作用,提高行业研发效率。接下来,探序将通过与大型药企联合开发、为药企/科研机构提供有价值的早期资产等方式进行商业化。希望通过IntelliFold的应用和持续升级,提升新药早期研发的成功率,改变新药研发“10年周期、10亿美元、10%成功率”的困境。
黄仁勋“通过AI,像设计芯片一样设计蛋白质和药物”的理念在美国已被广泛接受。随着AI的应用,临床前和处于临床一期的药物资产价值正在重估。因为AI的介入,这些早期资产的成药概率大大增加。诺华全球CEO瓦斯·纳拉辛汉曾表示,希望AI等新技术能将药物研发的成功率从现在的1/10提升到2/10、甚至3/10。
本文仅代表作者观点,版权归原创者所有,如需转载请在文中注明来源及作者名字。
免责声明:本文系转载编辑文章,仅作分享之用。如分享内容、图片侵犯到您的版权或非授权发布,请及时与我们联系进行审核处理或删除,您可以发送材料至邮箱:service@tojoy.com




