重磅,首款国产干细胞产品获批上市
"在严肃的医疗中,干细胞产品已经被批准,在美容、抗衰老等消费医疗领域的批准也将走上倒计时。"
干细胞治疗领域在生命科学创新的浪潮中迎来了突破!
从国家美国食品药品监督管理局官网了解到,国内首款干细胞疗法产品——艾米迈托赛注射剂(商品名称:睿铂生)一月二日正式获批上市,该产品特别能治疗激素治疗失败的急性移植物抗宿主病(以下简称:aGVHD)。

起源于国家美国食品药品监督管理局官网
值得注意的是,2024年12月18日,美国美国食品药品监督管理局在这款干细胞产品获得批准之前,(FDA)也批准了第一种基于胚胎干细胞的治疗方法——Ryoncil(Remestemcel-L),这种治疗方法专门用于治疗类固醇难治性aGVHD。

起源于FDA官网
短短半个月,中美干细胞产品不断获得批准,这不仅是干细胞行业划时代价值的重大进步,也是干细胞治疗从技术时代向商品时代迈进的关键里程碑。同时,对美容行业也具有重要意义,在一定程度上可以为干细胞技术在医疗美容应用领域的转型提供重要的实践基础。
国内首款干细胞药物紧随FDA获准。
公开资料显示,aGVHD是一种多器官综合征,在异基因造血干细胞移植后,由供应商的淋巴细胞攻击受者组织,可累及皮肤、肝脏、胃肠道等器官,甚至在病情严重时死亡。
Ryoncil,中美干细胞产品。、通过独特的免疫调节和修复功能,艾米迈托赛的不断出现,为aGVHD患者带来了新的治疗选择,有助于缓解aGVHD的临床表现,从而提高患者的生活质量。
Ryoncil作为世界上第一种针对aGVHD的胚胎干细胞疗法,是由美国Mesoblast公司开发的,专门为类固醇难治性aGVHD2个月以上儿童。。据了解,Ryoncil是来自同一异体骨髓的间充质基质细胞。T细胞介导的炎症反应可以通过抑制T细胞增殖和减少炎症细胞因子和干扰素的产生来调节。

来自Mesoblast官网
回首获准过程,尽管Ryoncil最终成功上市,但Ryoncil的道路并不容易。起初,Prochymal(后来更名为Remestemcel-L)美国Osiris产品 Therapeutics拥有这家公司,尽管它在2010年获得了I型糖尿病孤儿药的潜在资格,但它在美国的上市过程却频频受挫。2024年12月18日,Mesoblast公司接力,继续深耕研发,率先在加拿大、新西兰、日本等国取得突破,最终获得FDA许可,正式进入美国市场。
2025年1月2日,中国艾米迈托赛注射剂获批上市,成为中国第一种干细胞药物。据悉,该药物由铂生卓越生物科技(北京)有限公司开发,主要适用于超过14岁的aGVHD患者,主要是消化道受累导致的激素治疗失败。,填补了国内干细胞治疗药物的空白。
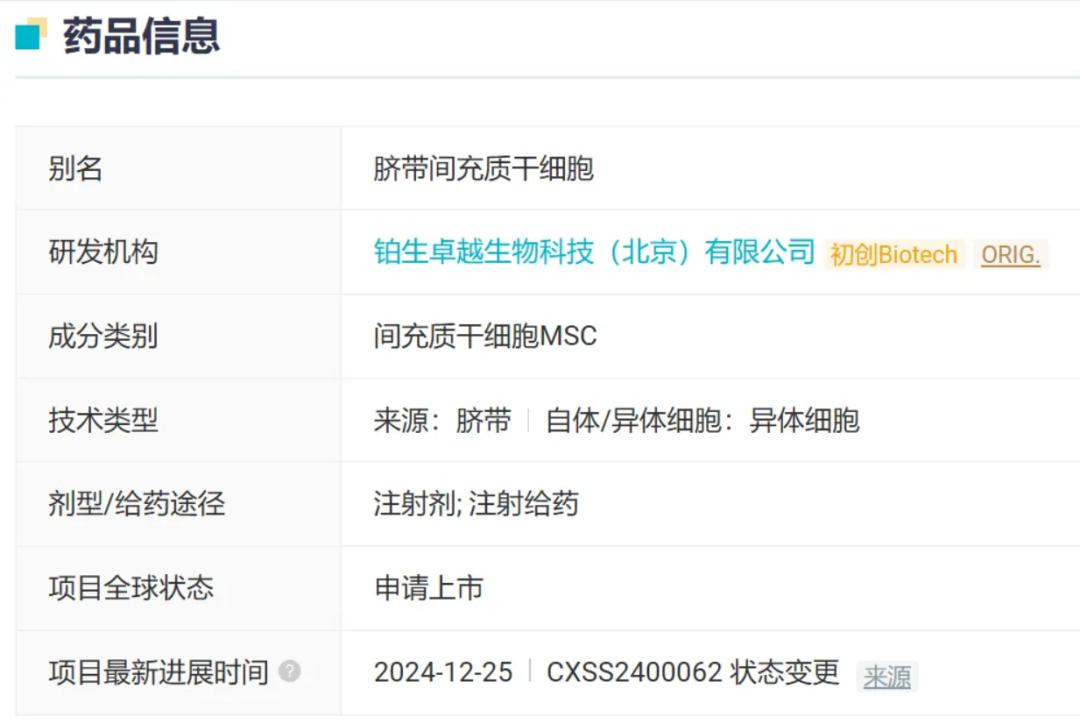
药物基本信息“艾米迈托赛”(来自Insight 数据库)
早在2013年3月,这种药物的研究人员就在国内提交了新药临床研究申请。(IND),然而,当时由于监管政策处于起步阶段,临床试验许可直到2020年6月才获得。之后花了4年时间才在2024年6月被药品评审中心列为优先审批,最终于于同月25日正式提交了注册上市申请。(NDA),出现在受理队列中。
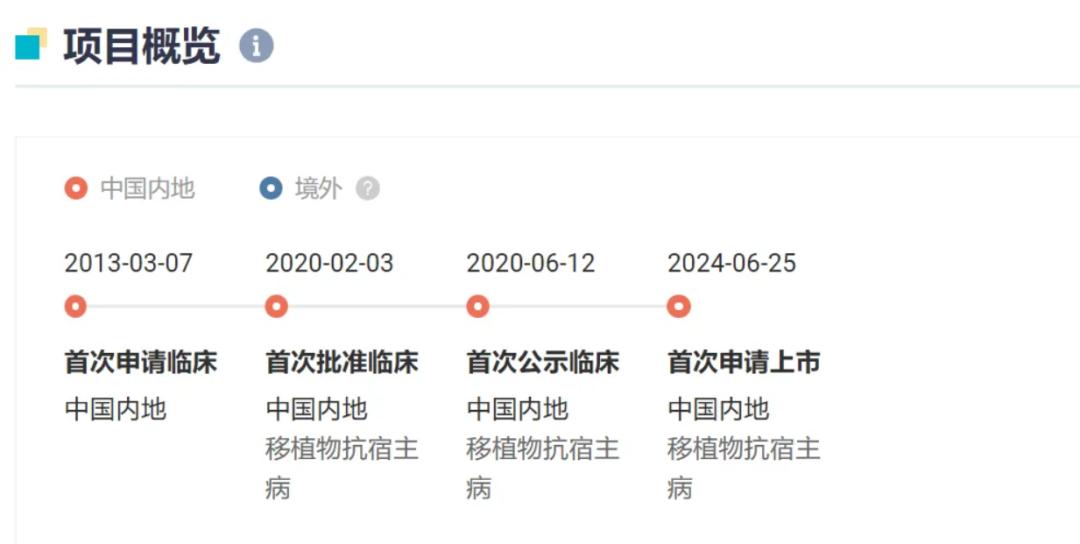
关键注册节点“艾米迈托赛”(来自Insight 数据库)
现在,艾米迈托赛最终在新年伊始获得国家美国食品药品监督管理局的许可,成为中国第一种干细胞治疗药物。目前已经完成。 II 期限临床试验,III 期临床试验也在稳步推进。而且值得注意的是,这种药物将作为处方药上市,相应的疾病可以通过医院的医生处方来治疗。
从技术角度对比中美两款干细胞产品不难看出,两者都集中在一起。胚胎干细胞,这类干细胞起源于中胚层,广泛分布于人体细胞器官,如骨髓、脐带、脐带血和脂肪,具有多向分化的优异潜力,五大显著特征包括自我复制、低抗原、高活性、抑炎性和不成瘤性。,前沿研究表明,再生医学和细胞治疗的应用潜力巨大。
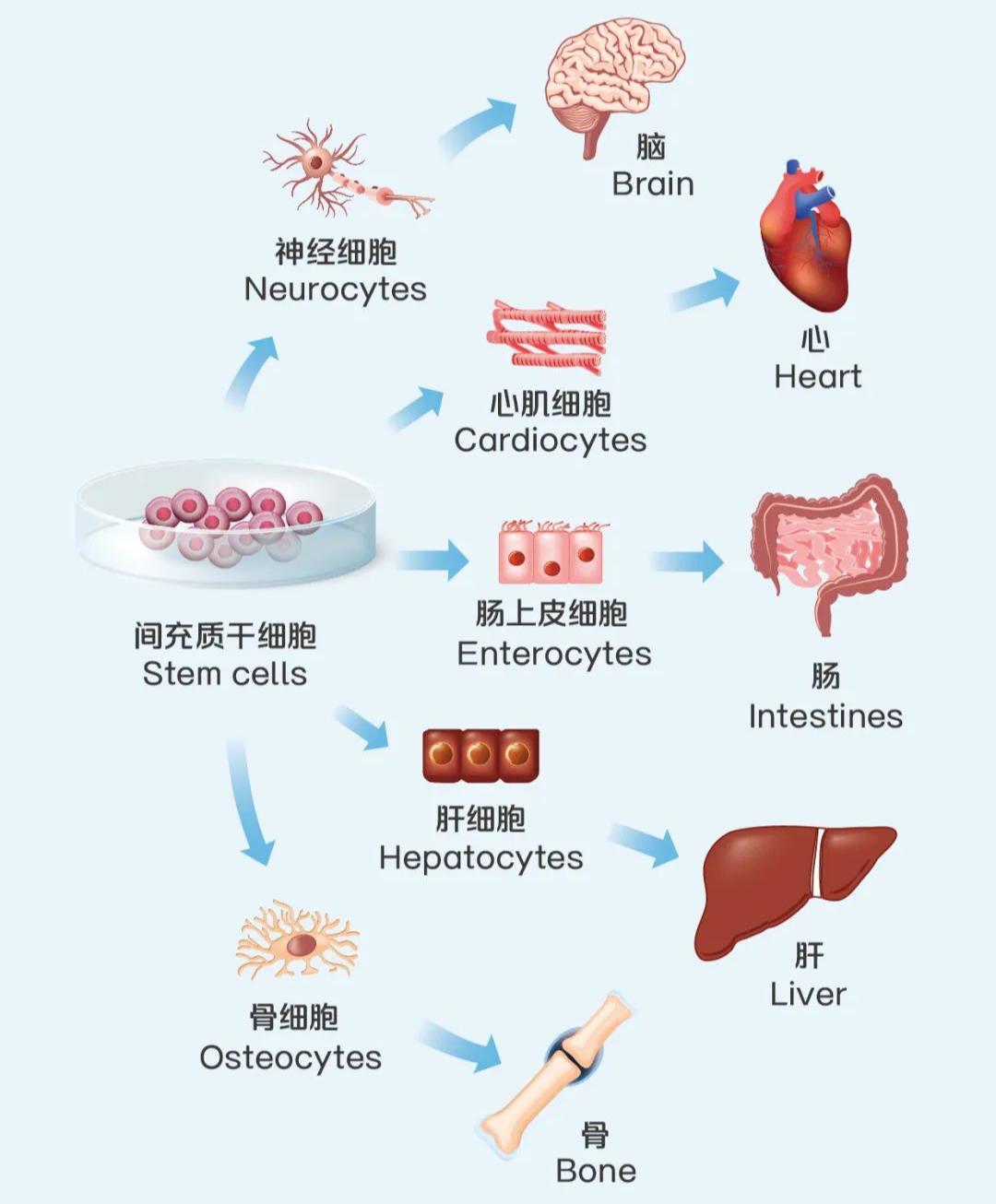
胎儿干细胞分化图(来自华大细胞)
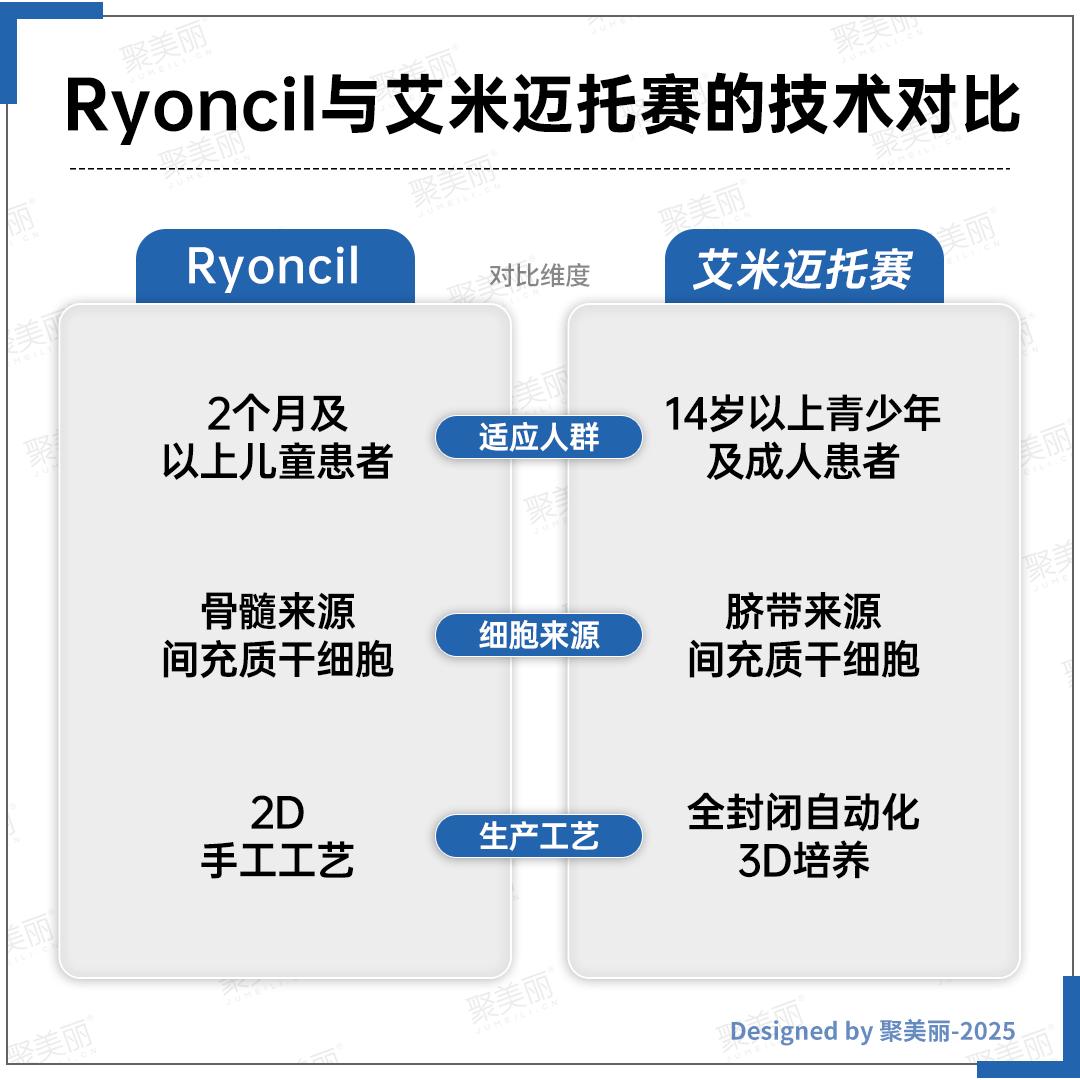
而且从下图可以看出,与Ryoncil相比,艾米迈托赛有三个显著的技术优势:
1、取材更方便:骨髓间充质干细胞与Ryoncil相比, 胚胎干细胞来源的脐带材料更加方便。
2、更广泛地适应群体:艾米迈托赛可以适用于14岁以上的人群,而Ryoncil只适用于2个月以上的儿童患者。
3、生产工艺更加先进:与Ryoncil的2D手工工艺相比,艾米迈托赛采用全封闭自动3D培训,具有较好的生产效率和稳定性。
以上代表着,虽然中国在化学和生物药物方面在过去几十年中处于全面落后的地位,但随着国内艾米迈托赛的获准,中国似乎已经可以与美国等新药研究大国“掰手腕”,尤其是在细胞领域。
政策/市场双驱动,干细胞治疗进入快车道
虽然在干细胞治疗领域取得了很大的进步,但回顾过去,我国干细胞产业的发展并不平坦。多年来,虽然临床应用领域不断推广,但真正到达临床后期并上市的商品寥寥无几。
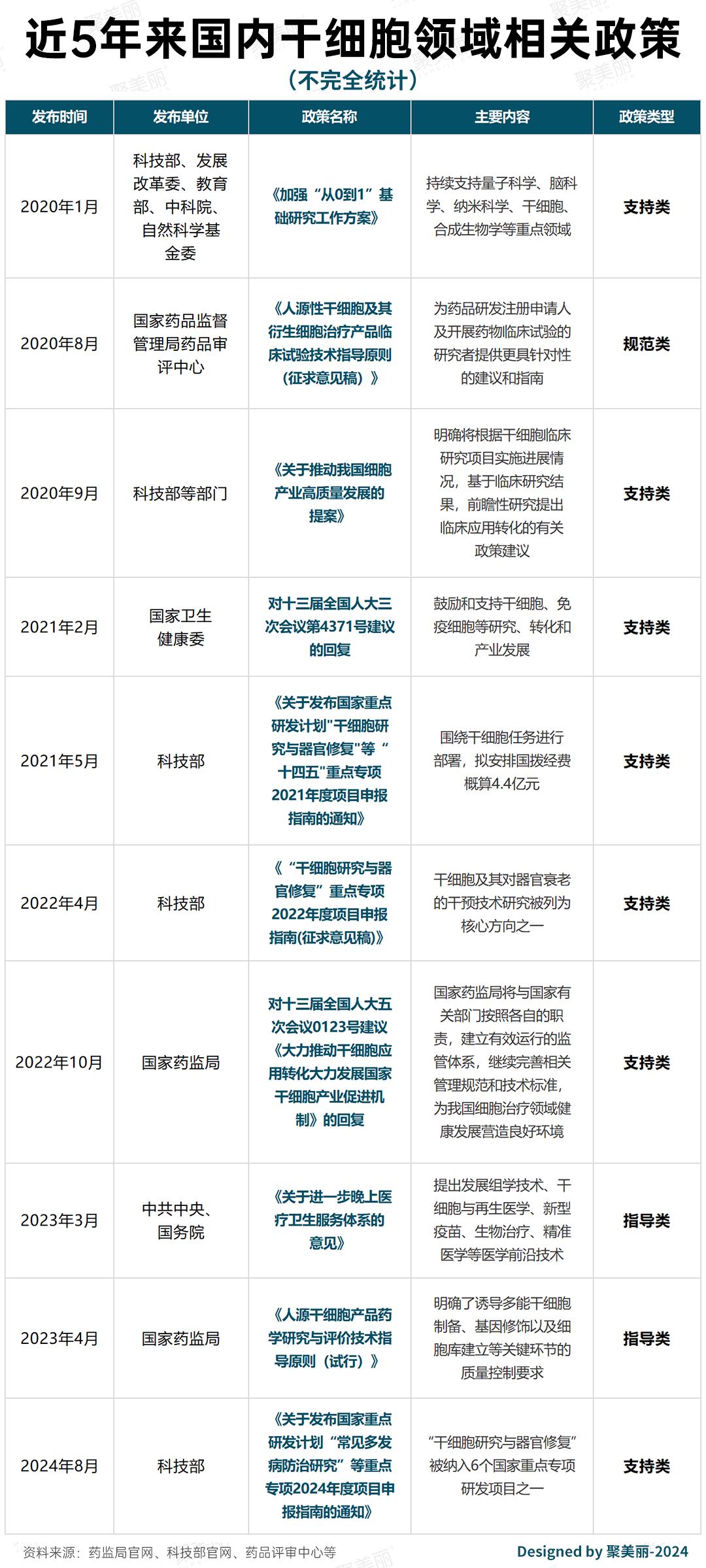
这一次,中国可以获批上市第一种干细胞治疗。事实上,它与我国近年来大力鼓励和支持干细胞实验研究和临床转化的重大突破密切相关。
就政策而言,百傲再生COO任敏华对于聚美丽来说,干细胞是我国战略导向中非常重要的一个方向。近年来,我国出台了许多促进干细胞临床研究和相关产品开发应用的政策。
而且从行业规模来看,在全球范围内,干细胞治疗市场呈现出快速增长的趋势。根据Research and 根据Markets的报告,预计未来几年,全球干细胞治疗市场将以超过15%的复合增长速度增长。而且在我国,干细胞治疗的市场发展更加迅速。根据南方财富网的数据,到2025年,中国干细胞医疗市场预计将达到126亿美元,复合增长率为19.1%。
随着政策利好和市场需求的推动,我国干细胞产业发展迅速。根据国家美国食品药品监督管理局药品审评中心副主任的说法。王涛从2017年开始,到现在,我国共有120多种干细胞(药物)被允许进入临床试验阶段,其中包括血液系统、呼吸道、心血管系统和一些自身免疫性疾病。
起源于东方时空
此外,根据医学研究登记信息系统和卫生健康委官网的数据,截至目前,我国已受理106种干细胞药物的临床试验申请,其中默认进入临床试验的79种,国内已批准设立141家干细胞临床研究备案机构(含部队医院)。
"未来5-10年,我们国家的干细胞临床转换将迎来发展的‘黄金期’。“南方科技大学恒普生命科学研究中心首席临床医学专家李定纲如果是预测道。就像李定纲据说,在政策和市场的双重推动下,中国干细胞产业正进入快速发展的新阶段,这无疑将为干细胞技术在复杂疾病治疗和应用领域的应用开辟新的可能性。
不仅仅是疾病治疗,干细胞治疗的可能性更大
干细胞药物迎来了合规化的曙光,但是这和医美,甚至化妆品行业到底有什么关系吗?
事实上,干细胞疗法并不局限于严肃的医疗领域,如疾病治疗,在美容、抗衰老等消费医疗领域也有很大的作用。。一些研究已经证明,胚胎干细胞可以有效改善皮肤松弛、皱纹等衰老症状,这意味着干细胞治疗也有望为美容行业带来全新的解决方案。
但是,从科学的角度来看,干细胞在抗衰老和美容领域的研究仍然停留在实验室鼠标、文献研究和小样本研究的临床实践中,仍然缺少更强级别的科学证据作为支撑。到目前为止,干细胞临床试验与美容、抗衰老相关的研究几乎为零,换句话说,在抗衰老和美容方面,干细胞的合规发展尚不明朗。。
但总的来说,我们有理由相信,干细胞虽然还处于医疗美容和抗衰老领域的初步研究阶段,但在国内首款干细胞药物获批的重要时间节点,其合规应用仍值得期待,就像 CEO北京茉莉数据网络科技有限公司MOLY晓东这段视频说:“在严肃的医疗中,干细胞产品得到了批准,在美容、抗衰老等消费医疗领域实际上也走上了倒计时。”
本文来自微信微信官方账号“聚美”(ID:jumeili-cn),作者:沐沐,36氪经授权发布。
本文仅代表作者观点,版权归原创者所有,如需转载请在文中注明来源及作者名字。
免责声明:本文系转载编辑文章,仅作分享之用。如分享内容、图片侵犯到您的版权或非授权发布,请及时与我们联系进行审核处理或删除,您可以发送材料至邮箱:service@tojoy.com







