首个千人癌症疫苗试验计划启动,肿瘤治疗迎来“里程碑时刻”
加星标,不要错过每日推送!方法见文末动图
人类可能从治愈癌症的目标上迈出了一大步。这一次,主角是癌症疫苗。中国英国的医疗服务体系正在启动一个大规模的计划,要在全国范围内招募1000多名癌症患者,并通过匹配迅速将其纳入癌症疫苗的临床试验。这是世界上第一个这样的计划。目前已有数十名癌症患者纳入启动计划。
由于其极强的特异性,癌症疫苗准确靶向癌细胞,不伤害“无辜”;它还可以使患者的免疫系统牢记癌细胞的特性,有望为患者提供持久的保护,避免癌症复发。这是人群的“里程碑时刻”。
发文 | 木木
癌症是世界上最重要的死亡原因之一,每年造成数百万人死亡。虽然医疗技术在不断进步,但手术、化疗、放疗等常见的癌症治疗方法仍有许多限制和副作用。
近年来,一项创新技术旨在提供永久治愈癌症,可以通过激发免疫系统来识别和攻击癌细胞,避免癌症复发。这是癌症疫苗,在癌症治疗领域被称为“改变游戏规则”。
最近,英国我国的医疗服务体系(NHS)开展了一项开创性的个性化癌症疫苗临床研究,又称“” matchmaking “计划旨在为每个患者量身定制癌症疫苗。这种疫苗只需要几个星期就能完成,可以通过引导患者自己的免疫系统来寻找和杀死癌细胞。
研究小组表示,符合筛选标准并同意接受血液检测和癌症组织样本分析的患者将有机会立即参与世界上第一个计划,这也让许多患者看到了癌症治疗的新曙光。
改变游戏规则的人
癌症疫苗作为癌症防治领域的一大突破技术,希望通过刺激人体自身的免疫系统,特别是 T 对抗癌细胞的细胞。
众所周知,T 细胞是免疫系统中识别和消除异常细胞的关键免疫细胞。通常,我们通过接种疫苗来刺激和增强免疫细胞的功能,使其能够辅助治疗特定的病原菌。
癌症疫苗也是如此,可以分为预防性疫苗和治疗性疫苗。预防性疫苗旨在避免某些病毒感染引起的癌症,例如 HPV 疫苗用于预防宫颈癌;治疗性疫苗用于帮助免疫系统识别和攻击已经发生的肿瘤。
但与某些疾病的疫苗不同,癌症疫苗的一个重要目标是克服肿瘤微环境。(TME)免疫抑制在里面。TME 有大量的免疫抑制细胞和分子,例如调节性 T 细胞(Tregs)、髓原性抑制细胞(MDSCs)以及抑制性细胞因子(例如 TGF- β、IL-十)它们能抑制免疫系统的抗肿瘤反应。
所以,通过接种癌症疫苗,可提高效果。 T 减少免疫抑制细胞的影响,改善细胞活性, TME,从而更有利于免疫系统攻击癌细胞。另外,癌症疫苗还可以通过“抗原扩展”现象来增强免疫反应。所谓“抗原扩展”,即免疫系统不仅会对目标抗原产生反应,还会识别和攻击其他肿瘤抗原,进一步扩大免疫反应的广度和强度。
癌症疫苗技术相对于传统的化疗和放疗而言,具有显著的优势。
一是特异性强,能准确靶向癌细胞,不损伤周围正常细胞,大大降低治疗副作用;第二,疫苗接种后,免疫系统会牢记癌细胞的特点,有望为患者提供更持久的保护,防止癌症复发;其次,癌症疫苗可以通过识别和针对每个患者独特的癌细胞突变来实现个性化治疗,并提供量身定制的治疗方法;此外,肿瘤疫苗还可以与其它治疗方案协同作用,提高整体治疗效果,给病人带来更多的生存希望。
癌症疫苗不仅在增加患者生存期方面表现出巨大的潜力,而且可以显著提高患者的生活质量。与传统的化疗和放疗不同,癌症疫苗的副作用较小,患者在治疗过程中可以保持更好的生活质量。
所以,近几年来,随着研究的深入,癌症疫苗已在众多基础研究中展现出一丝治愈癌症的曙光。
肿瘤个性化疫苗试验计划
对此次开始的大规模肿瘤个性化疫苗临床研究,NHS 阿曼达负责人 · 普里查德认为,这是病人的“里程碑时刻”。
目前,NHS 已经招募了数十名患者参与癌症疫苗启动计划,后续计划在英格兰各地进行。 30 个 NHS 网站招募了1000多名患者。第一批患者的实验将重点关注结直肠癌、皮肤病、肺癌、膀胱癌、胰腺癌和肾癌,未来将扩展到其他类型的癌症。
伊恩恩恩恩,英国癌症研究中心的研究与创新执行总监 · 福克斯说,患者获得个性化疫苗接种“令人兴奋”,这将成为抗癌斗争的“游戏规则改变者”。他强调:“这样的临床试验对于帮助更多的人活得更久,活得更好,摆脱对癌症的恐惧尤为重要。”
首先加入癌症疫苗研究计划 NHS 患者,名叫 Elliot Pfebve。这位 55 年考文垂大学讲师一向身体健康,但在接受全科医生常规体检时,被诊断为结直肠癌。所以,他接受了肿瘤切除术,切除了肿瘤。 30 大肠厘米,并且接受化疗。接着,他在伯明翰大学医院。 NHS 该基金将接种此类个性化癌症疫苗。
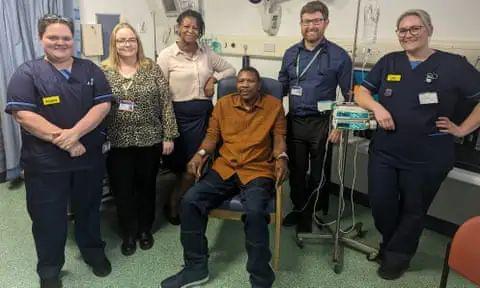
图:Elliot Pfebve(中)是首个加入癌症疫苗计划的人。 NHS 病人来源:University Hospitals Birmingham NHS foundation trust
"参加这个实验是我一生中一个很重要的决定,对于我和我的家人来说都是如此。" Pfebve 说。“在经历了诊断困难和虚弱的化疗后,我能够参加一个可能带来新癌症治疗的实验。我觉得很棒。如果别人能从实验的发现中受益,那就更好了。”
在一个有趣的点上,这种疫苗的设计采用了辉瑞 /BioNTech 开发新冠疫苗也是如此 mRNA 疫苗技术。
当今疫苗研发的前沿方向,DNA 疫苗和 RNA 疫苗因其独特的优点而备受关注。
DNA 通过引进特定肿瘤抗原的疫苗技术 DNA 将其序列到宿主细胞中,使细胞表达这些抗原,从而引发免疫反应。它的高稳定性、大规模生产的便利性和编码各种抗原的能力为肿瘤免疫治疗提供了新的途径。然而,DNA 仍有待提高疫苗的递送效率和表达水平。
RNA 疫苗则利用 mRNA 将分子直接翻译成体内的抗原蛋白,从而有效地诱发免疫反应。RNA 疫苗不需要进入细胞核的特点也赋予了其高表达效率,生产工艺简单方便,非常适合应对突变谱不断变化的肿瘤(类似于新冠肺炎的快速突变)。然而,RNA 由于稳定性低,为了保证其有效性和安全性,需要使用脂类纳米颗粒等载体进行保护和传递。
图:mRNA 疫苗技术来源:Donny Bliss/NIH
在前沿疫苗研发领域,还有一种创新的方法——生成肽(SLP)疫苗。它利用生长肽,通过体内输送系统将其引入体内。这种肽含有多种 T 能同时激活细胞表位 CD4 和 CD8 T 细胞,诱发强大的免疫反应。SLP 疫苗具有高度特异性和可定制性的优点,可根据病人的肿瘤特异性突变进行设计。然而,SLP 接种疫苗的生产成本很高,而且还需要精确的递送系统来保证有效性。
挑战和新进展
尽管癌症疫苗在肿瘤治疗领域具有巨大的潜力,但其开发和应用过程仍然充满了许多复杂而艰巨的挑战。这不仅涉及如何选择合适的抗原,还涉及到应对肿瘤细胞免疫逃逸机制、改善肿瘤微环境、优化疫苗交付平台等各个方面。
尽管面临这些挑战,但癌症疫苗领域仍在迅速发展。伴随着科技的不断发展,特别是新技术、新工具的出现,许多挑战和难题正在一点一点地被打破。
举例来说,随着下一代测序技术的不断发展,通过测序病人的肿瘤 DNA 和 RNA,能迅速准确地识别病人的肿瘤基因变异,从而设计出相应的疫苗。治疗癌症疫苗的成功主要取决于疫苗中抗原的特性,尤其是发现更多潜在的新抗原。新抗原是由肿瘤基因变异引起的蛋白质片段,不同于正常细胞中所表达的蛋白质,因此免疫系统可将其识别为外来物质。
此外,近年来计算生物学和生物信息学的发展也使得个性化癌症疫苗的设计更加可行。癌症是一种高度异质的疾病,不同患者的肿瘤具有不同的突变谱和免疫特性。因此,个性化癌症疫苗的思路是根据每个患者的具体情况设计特定的抗原和治疗方法。显然,这种个性化的解决方案需要生物信息技术的强有力支持。
一般来说,近几十年来,治疗性癌症疫苗取得了显著发展。尽管面临许多挑战,但随着肿瘤免疫系统的深入了解和新技术的发展,疫苗设计和提交平台得到了改善。治疗性癌症疫苗有望通过优化抗原选择、增强免疫反应、克服免疫逃逸机制、探索组合治疗策略,成为未来癌症治疗的重要组成部分。
此外,癌症疫苗的研究和发展也促进了我们对免疫系统和癌症生物学的理解。通过分析癌症疫苗是如何工作的,科学家可以深入了解如何识别和攻击免疫系统中的癌细胞,以及如何避免免疫监测。这些内容不仅可以帮助开发更高效的癌症疫苗,还可以用于其他类型的免疫治疗。
有理由认为,随着研究的不断推进,癌症疫苗将成为抗击癌症的重要武器,为人们战胜这一重大疾病带来曙光。
参考资料
[ 1 ] https://www.theguardian.com/science/article/2024/may/31/nhs-patients-in-england-to-be-offered-trials-for-world-first-cancer-vaccine
[ 2 ] https://www.theguardian.com/science/article/2024/may/31/what-are-cancer-vaccines-and-have-scientists-finally-found-a-cure
[ 3 ] Wang SS, Liu W, Ly D, Xu H, Qu L, Zhang L. Tumor-infiltrating B cells: their role and application in anti-tumor immunity in lung cancer. Cell Mol Immunol. 2019;16 ( 1 ) :6-18. doi:10.1038/s41423-018-0027-x
[ 4 ] Mollica Poeta V, Massara M, Capucetti A, Bonecchi R. Chemokines and Chemokine Receptors: New Targets for Cancer Immunotherapy. Front Immunol. 2019;10:379. Published 2019 Mar 6. doi:10.3389/fimmu.2019.00379
[ 5 ] Balan S, Radford KJ, Bhardwaj N. Unexplored horizons of cDC1 in immunity and tolerance. Adv Immunol. 2020;148:49-91. doi:10.1016/bs.ai.2020.10.002
[ 6 ] Ruhland MK, Roberts EW, Cai E, et al. Visualizing Synaptic Transfer of Tumor Antigens among Dendritic Cells. Cancer Cell. 2020;37 ( 6 ) :786-799.e5. doi:10.1016/j.ccell.2020.05.002
[ 7 ] Roberts EW, Broz ML, Binnewies M, et al. Critical Role for CD103 ( ) /CD141 ( ) Dendritic Cells Bearing CCR7 for Tumor Antigen Trafficking and Priming of T Cell Immunity in Melanoma. Cancer Cell. 2016;30 ( 2 ) :324-336. doi:10.1016/j.ccell.2016.06.003
[ 8 ] Ott PA, Hu Z, Keskin DB, et al. An immunogenic personal neoantigen vaccine for patients with melanoma [ published correction appears in Nature. 2018 Mar 14;555 ( 7696 ) :402 ] . Nature. 2017;547 ( 7662 ) :217-221. doi:2299110.1038/nature
[ 9 ] Appay V, Jandus C, Voelter V, et al. New generation vaccine induces effective melanoma-specific CD8 T cells in the circulation but not in the tumor site. J Immunol. 2006;177 ( 3 ) :1670-1678. doi:10.4049/jimmunol.177.3.1670
生产:中国科普
相关阅读
1
2
3
4
5
最近推荐
1
2
3
4
5
特 别 提 示
1. 进入『返朴』微信公众号底部菜单“精品栏目”,可以查看不同主题系列的科普文章。
2. 『返朴』提供每月搜索文章的功能。关注微信官方账号,回复四位数组成的年份。 月份,如" 1903 ",可获取 2019 年 3 月文章搜索,以此类推。
找不到《返朴》?快加星标!!
长按照下面的照片注意「返朴」,看看更多的历史文章
微信实行乱序推送,常点"在看",可以防止失联
本文仅代表作者观点,版权归原创者所有,如需转载请在文中注明来源及作者名字。
免责声明:本文系转载编辑文章,仅作分享之用。如分享内容、图片侵犯到您的版权或非授权发布,请及时与我们联系进行审核处理或删除,您可以发送材料至邮箱:service@tojoy.com





